| 2024年3月13日 酸化的リン酸化の抑制がFOPの新たな治療法に繋がる可能性 |
孫麗萍1、金永輝1*、西尾恵2、渡辺真3、鎌倉武史1、永田早苗2、福田真幸1、前川裕継2、川井俊介2、山本拓也2, 4, 5、戸口田淳也1, 2*
*責任著者
(1京都大学医生物学研究所、2京都大学iPS細胞研究所、3島津製作所ライフサイエンス研究所、4京都大学ヒト生物学高等研究拠点、5理化学研究所革新知能統合研究センター)
Oxidative phosphorylation is a pivotal therapeutic target of fibrodysplasia ossificans progressiva
Life Science Alliance 7, 5 (2024); https://doi.org/10.26508/lsa.202302219
概要
孫麗萍 京都大学医生物学研究所博士課程学生、金永輝 同研究所助教らは、戸口田淳也 京都大学iPS細胞研究所(CiRA)特定拠点教授との共同研究により、難治性疾患である進行性骨化性線維異形成症(Fibrodysplasia Ossificans Progressiva、FOP)における異所性骨化に酸化的リン酸化(Oxidative Phosphorylation、OXPHOS)(注1)が深く関与しており、OXPHOSの抑制が新しい治療法に繋がることを明らかにしました(図1)。
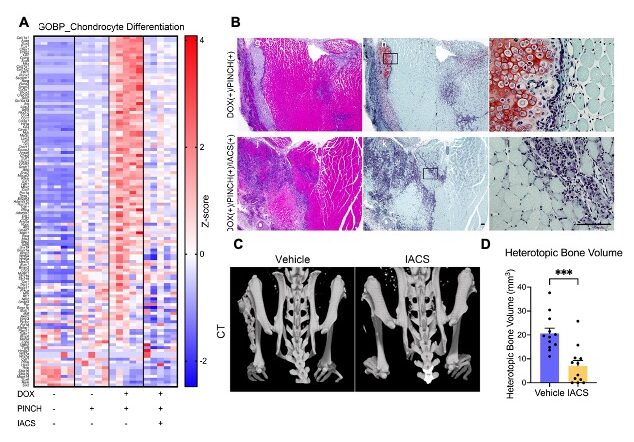
図1:FOPモデルマウスにおける外傷誘導性異所性骨化に対する酸化的リン酸化の阻害剤IACS-010759(注6)の抑制効果。
A:誘導7日目の軟骨分化関連遺伝子の発現。B:誘導7日目の組織像。C:誘導21日目のCT像。D:異所性骨の定量解析。
FOPは骨形成因子の受容体であるACVR1(注2)遺伝子の変異が原因で、骨格筋、腱、靱帯などの軟部組織の中に異所性骨と呼ばれる骨組織が形成され、四肢体幹の運動が著しく障害される疾患です。これまでに戸口田研究室では池谷真准教授(CiRA)との共同研究として、FOP患者さん由来のiPS細胞から誘導した間葉系幹細胞(Mesenchymal stem cell、MSC)(注3)を活用した研究により、異所性骨化を引き起こす物質としてActivin A(注4)を同定し、Activin Aが変異型ACVR1受容体を介してmTORC1(注5)を活性化し、MSCを軟骨細胞に分化させ、異所性骨化を誘導することを明らかにしました。しかし、mTORC1の活性化がどのようにしてMSCを軟骨に分化させるのかは不明でした。
そこで、Activin Aによる軟骨分化の過程におけるMSCの遺伝子発現を解析したところ、mTORC1シグナルと共にOXPHOSシグナルが活性化していることが判明しました。そしてOXPHOS阻害剤によりMSCの軟骨分化が抑制されることから、Activin Aによる軟骨分化誘導にOXPHOSの活性化が必要であることが判明しました。更にFOPモデルマウスを用いたin vivoの実験により、異所性骨化の過程で局所においてOXPHOSが活性化されており、OXPHOS阻害剤により異所性骨化が抑制されました。これらの結果はFOPにおける異所性骨化の発生機構の理解に貢献することに加えて、OXPHOSがFOPに対する新しい治療標的となり得ることを示す結果であると考えられます。
本研究成果は、2024年2月16日に、国際学術誌「Life Science Alliance」にオンライン掲載されました。
(注1)酸化的リン酸化
電子伝達系に共役して起こる一連のリン酸化(ATP合成)反応。 細胞内で起こる呼吸に関連した現象で、高エネルギー化合物のATPを産生する回路の一つ。
(注2)ACVR1
BMPの受容体を構成するタンパク質で、BMPと結合することで下流の分子を活性化する。
(注3)間葉系幹細胞
骨・軟骨・脂肪細胞などといった間葉系の細胞に分化する能力を持った間質細胞。
(注4)Activin A
トランスフォーミング増殖因子β(Transforming Growth Factor β、TGF-β)スーパーファミリーに属するタンパク質で、細胞増殖や分化など多くの活性作用を持つ。
(注5)mTORC1(mechanistic target of rapamycin complex 1)
栄養素・エネルギー・酸化還元状態のセンサーとして機能し、タンパク質合成を制御するタンパク質複合体。
(注6)IACS-010759
ミトコンドリアのNADH-キノン酸化還元酵素(呼吸鎖複合体-I)に対する阻害剤。
