| 2019年4月11日 CRISPRスクリーニングによるがん治療薬候補の網羅的同定 |
Fiona M. Behan 1,2、Francesco Iorio 1,2,3、Gabriele Picco 1、Emanuel Gonçalves 1、Charlotte M. Beaver 1、Giorgia Migliardi 4,5、Rita Santos 6、Yanhua Rao 7、Francesco Sassi 4、Marika Pinnelli 4,5、Rizwan Ansari 1、Sarah Harper 1、David Adam Jackson 1、Rebecca McRae 1、Rachel Pooley 1、Piers Wilkinson 1、Dieudonne van der Meer 1、David Dow 2,6、Carolyn BuserDoepner 2,7、Andrea Bertotti 4,5、Livio Trusolino 4,5、Euan A. Stronach 2,6、Julio SaezRodriguez 2,3,8,9,10、遊佐宏介 1,2,11、Mathew J. Garnett 1,2
(1 Wellcome Sanger Institute, 2 Open Targets, 3 European Molecular Biology Laboratory, 4 Candiolo Cancer InstituteFPO, 5 Department of Oncology, University of Torino, 6 GlaxoSmithKline Research and Development, Stevenage, 7 GlaxoSmithKline Research and Development, Collegeville, 8 Faculty of Medicine, RWTH Aachen University, 9 Institute for Computational Biomedicine, Heidelberg University, 10 Heidelberg University Hospital, 11 京都大学ウイルス・再生医科学研究所幹細胞遺伝学分野)
”Prioritization of cancer therapeutic targets using CRISPR-Cas9 screens”
概要
がんは過去約40年間日本人の死因第一位で、三大成人病と言われるがん、心疾患、脳血管疾患のうち、がんのみで死亡数、罹患率の上昇が続いています。その治療法は、外科的切除の他には、抗ガン剤や放射線治療といった正常細胞をも傷つけてしまう方法が主体です。近年、がん細胞の増殖や転移に関する分子機構の理解が進み、これらに関わる遺伝子産物の機能を特異的に抑制する分子標的薬の開発・臨床応用が進んでいます。がん細胞を狙い撃ちするため、正常細胞への毒性が従来の治療法に比べ少ない利点があります。これらに加え、現在ではがん免疫療法の導入も進んでいます。利点の多いがん分子標的薬ですが、その開発には1剤あたり200〜300億円もの多額の費用と10年以上に及ぶ長い時間を必要とし、また90%の新薬開発計画は途中で中止されてしまうという非常に難しいものです。新薬開発の成功率を上げ、がん患者さんにより多くの新薬を届けるには、最初により良い創薬標的の候補を選定することが重要です。
この研究では、ゲノム編集技術CRISPR-Cas9を用いた全遺伝子スクリーニング法(参考文献1,2)を30種類を超える324細胞株において実施し、各がん細胞株における細胞の生存・増殖に必須の遺伝子のプロファイルの取得に成功しました。この必須遺伝子プロファイルを元に様々なコンピューター解析を行い、各がん種ごとの共通必須遺伝子、また、がん遺伝子変異の有無と相関関係を示す必須遺伝子等を新たに見出しました。さらに、これらの情報を統合することで各がん種において分子標的薬として有望と考えられる候補の絞り出しを行いました。
その結果、DNAミスマッチ修復機構欠損によってマイクロサテライト不安定性を示すがん(大腸がん、胃がんや卵巣がん等の一部に見られる)は、Werner症候群RecQヘリケース (WRN) を必要とすることが見出されました(図1)。この依存性はWRNヘリケース活性によるものであり、また、異種移植モデルにおいてWRN遺伝子を欠損させると腫瘍の退縮が見られること(図2)が実験的に確認され、WRNのヘリケース活性阻害剤がマイクロサテライト不安定性を示すがんに対する分子標的薬となる可能性が示されました。
この必須遺伝子プロファイルは全て公開しており、世界中のがん研究者、製薬会社に有用な情報を提供するものと考えられます。このデータの利用を通して、さらにがん細胞の増殖機構の科学的知見が得られ、新しい創薬につながることを研究チームは期待しています。
参考文献
(1) Koike-Yusa et al. Nature Biotechnology 32, 267-273 (2014)
(2) Tzelepis et al. Cell Reports 17, 1193-1205 (2016)
|
|
|
|
図の説明
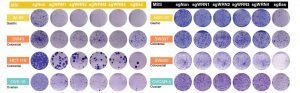
図1. マイクロサテライト不安定性を示すがん細胞は増殖にWRNを必要とする。
マイクロサテライト不安定性(MSI)を示すがん細胞株IM-95 (胃がん)、SW48とHCT-116 (大腸がん)、OVK-18(卵巣がん)は、WRN遺伝子をCRISPR-Cas9システムによって遺伝子破壊すると (図中のsgWRN1〜4の列)、細胞増殖が抑制され、通常時 (sgNon) と比べてコロニー形成能が有意に落ちる。一方、同様のがん種由来のマイクロサテライト安定 (MSS) 細胞株はWRN遺伝子を欠損しても増殖に影響がない。sgESSは、生存に必須の遺伝子を欠損されたコントロール。
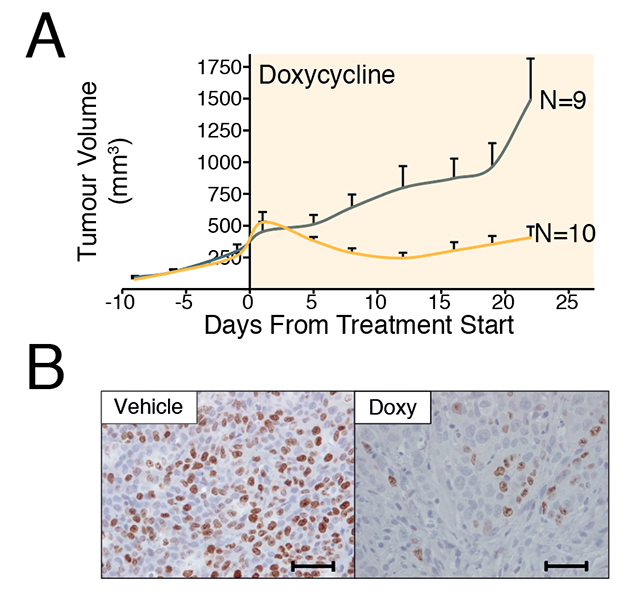
図2. WRN欠損は異種移植モデルにおいて腫瘍を退縮させる。
A. ドキシサイクリンにて発現誘導可能なsgWRNを組み込んだマイクロサテライト不安定性大腸がんHCT-116をマウス皮下に移植し、腫瘍が一定の大きさに達したところでWRNを欠損させた。WRN欠損後(図中、Doxycycline投与後)、腫瘍の有意な退縮が観察された。
B. WRN欠損後、腫瘍内でのKi67陽性細胞が有意に減少した。